خرید انواع اسید بصورت عمده و خرد در کیمیا اکسیر سازان کوثر بصورت اینترنتی و تلفنی امکان پذیر است.
اسید چیست؟
تعریف علمی: اسید به مادهای شیمیایی میگویند که یون هیدروژن یا پروتون بدهد یا الکترون جذب کند. بسیاری از اسیدها در ساختار شیمیایی خود با اتم هیدروژنی پیوند دارند که در اثر تفکیک در آب، کاتیون و آنیون آزاد میکند. هر قدر غلظت یون هیدروژن تولیدی بیشتر باشد، محلول، دارای خاصیت اسیدی بیشتر و pH پایینتری خواهد بود.
تعریف متفاوت دانشمندان در مورد اسید
تعریف آرنیوس از واکنش اسید-باز سبب توسعه نظریه هیدروژنی اسیدها شد و از آن برای تعریف جدید اسیدها و بازها استفاده میکنند. تلاشهای آرنیوس در این زمینه سبب شد تا جایزه نوبل شیمی را در سال ۱۹۰۳ کسب کند.
طبق تعریف، اسید آرنیوس به مادهای میگویند که در اثر تفکیک در آب، یون هیدروژن $$H ^ +$$ آزاد کند. به بیان دیگر، در محلولهای آبی، اسید، غلظت یونهای $$H ^ +$$ را افزایش میدهد. این پروتوندهی به آب، سبب تشکیل یون هیدرونیوم $$(H _ 3 O ^ +)$$ میشود.
مطالعه کنید: خطرناک ترین مواد شیمیایی جهان را بشناسید
طبق تعریف برونستد-لوری، اسید به مادهای میگویند که بتواند پروتون بدهد. این تعریف، محدودیت کمتری ایجاد میکند چراکه سایر حلالها به غیر از آب نیز در این تعریف دخیل هستند. به طور کلی، هر ترکیبی که بتواند پروتون از دست بدهد، اسید نام دارد. در این تعریف، آمینها و الکلها نیز جای میگیرند. تعریف برونستد-لوری، متداولترین تعریفی است که در خصوص اسیدها بکار برده میشود.
اسید لوییس به ترکیبی میگویند که بتواند با دریافت یک جفت الکترون، پیوند کووالانسی تشکیل دهد. طبق این تعریف، برخی از موادی که شامل هیدروژن نیستند هم به عنوان اسید شناخته میشوند. از جمله این مواد میتوان به آلومینیوم تریکلرید با فرمول $$(AlCl_3)$$ و بور تریفلوئورید با فرمول $$(BF_3)$$ اشاره کرد.

نحوه خرید اسید از کیمیا اکسیر کوثر
شما خریداران عزیز می توانید اسید مورد نظر خود را بصورت کاملا آنلاین خرید نمایید. بعد از ثبت سفارش خرید شما، همکاران ما در بخش حمل و نقل در سریع ترین زمان ممکن با توجه به شهر محل تحویل سفارش و همچنین میزان اسید خریداری شده، محصول را بدست شما خواهند رساند.
در بعضی از مواقع خریداران تمایل دارند که با کارشناسان فروش مجموعه قبل از خرید نهایی بصورت تلفنی صحبت داشته باشند. چرا؟
ممکن است برخی عزیزان به پروسه خرید آنلاین اسید آشنایی لازم را نداشته باشند.
سوالاتی در مورد محصول، غلظت آن، نحوه تحویل کالا و.... داشته باشند که جواب آن را در فروشگاه آنلاین کیمیا اکسیر کوثر پیدا نکرده باشند.
اگر چه امکان خرید بصورت مقدار بالا (تناژ) در سایت موجود است، اما برخی از خریداران در صورتی که سفارش خرید اسید تناژ داشته باشند، ترجیح می دهند که حتما بصورت تلفنی بعد از صحبت با کارشناسان فروش مجموعه ما ثبت سفارش خرید داشته باشند.
با توجه به صنعتی شدن زندگی و همچنین بالا رفتن سرعت و مهم بودن وقت و زمان اشخاص امروزه ترجیح اکثریت خریداران به یکی از دو روش ذکر شده می باشد. اما ما وظیفه خود می دانیم جهت رفاه حال مشتریان گرامی انواع روش های خرید را داشته باشیم. از این رو در صورتی که به هر دلیلی تمایل به خرید حضوری اسید داشته باشید این امکان برای شما میسر می باشد.

قیمت خرید اسید در کیمیا اکسیر کوثر
ما خود تولید کننده اسید نیستیم، اما به عنوان یکی از فروشندگان سطح یک در استان اصفهان توانایی تامین نیاز خریداران به انواع اسید را چه در سطح منطقه و چه در کل کشور داریم. مدیران مجموعه با تلاش های فراوان و اخذ مجوزهای مورد نیاز با عقد قرارداد با پتروشیمی های برتر کشور که در زمینه تولید اسید فعالیت دارند، این محصول را بصورت مستقیم با حذف انواع واسطه ها به فروش می رساند.
با توجه به همین موضوع قیمت خرید اسید در کیمیا اکسیر کوثر نسبت به شرکت های همکار در سطح استان اصفهان و حتی کشور ( به دلیل نزدیکی به پتروشی های تولید کننده اسید و حذف هزینه بسیار بالای حمل) مناسب تر می باشد.
شما چه نوع اسید هایی را تامین می کنید؟
مجموعه ما در کنار فعالیت در حوزه تولید انواع شوینده و ضد عفونی کننده استاندارد دامداری و مرغ داری ها، جهت تامین نیاز این مجموعه ها و دیگر مصرف کننده های اسید، تلاش کرده است انواع اسید پایه و اصلی را بصورت خرید عمده و خرد به مشتریان عرضه نماید. از جمله این اسید ها می توان به اسید سولفوریک 98 درصد، اسید کلریدریک 33 درصد صنعتی، اسید نیتریک صنعتی 64 و 55 درصد و دیگر اسید ها اشاره کرد.
آشنایی با ویژگی های شیمیایی اسید
- از نظر طعم ترش مزه هستند.
- اکثر اسیدها خاصیت خورندگی دارند.
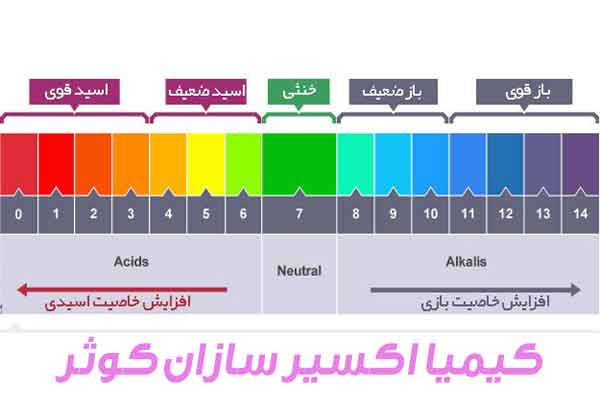
- سطح ph اسیدها بین 0 تا 6 متغیر است.
- اسیدها رنگ آبی را به قرمز تبدیل می کنند.
- اسید رنگ زرد را به صورتی تغییر می دهد.
- در هنگام واکنش با کربنات ها، دی اکسید کربن تولید می کنند.
- اسیدها در هنگام ترکیب با مواد قلیایی اسیدیته خود را از دست می دهند.

چند مدل اسید وجود دارد؟
میزان قدرت اسید رابطه مستقیم با میزان تفکیک شدن آن در آب و تولید یون است. اسید قوی به اسیدی میگویند که در حدود ۱۰۰ درصد آن در محلول، تفکیک شود. اسیدهایی همچون سولفوریک اسید و نیتریک اسید را نیز به عنوان اسیدهای قوی طبقهبندی میکنند. در شیمی هر اسیدی که برچسب اسید قوی دارد، حتما خیلی قوی و خورنده نیست.
عامل مهمی که در طبقه بندی قوی ترین اسید ها نقش دارد توانایی آنها در آزاد سازی یون های هیدروژن، در محلول معین است. زمانی که یک اسید قوی با آب مخلوط می شود، به طور کامل به یون هیدروژن و یک آنیون تجزیه می شود. به بیان ساده تر، مولکول های اسید قوی در محلول تجزیه می شوند و هر اسیدی که این قابلیت را نداشته باشد اسید ضعیف نامیده می شود. از طرفی واکنش اسیدهای قوی یک طرفه و بازگشت ناپذیر است.
اسیدهای «دو پروتونه» (Diprotic) و «چندپروتونه» (Polyprotic) میتوانند بیش از یک پروتون از دست بدهند اما مقدار «pKa» اسید قوی تنها مربوط به از دست دادن پروتون اول است.
مقدار pKa اسید قوی عددی کوچک و ثابت تفکیک آن یعنی «Ka» عددی بزرگ است. بسیاری از اسیدهای قوی خورنده هستند اما برخی از سوپراسیدها اینگونه نیستند. در مقابل، برخی از اسیدهای ضعیف مانند هیدروفلوئوریک اسید میتوانند به شدت خورنده باشند.
مهم ترین اسید های قوی

اسید ضعیف به اسیدی میگویند که به هنگام انحلال در آب، به طور کامل تفکیک نمیشود. استیک اسید (اتانوییک اسید) از جمله اسیدهای ضعیف به شمار میآید.
مهم ترین اسیدهای ضعیف
- اسید فسفریک
- هیدروفلوئوریک اسید
- نیتروس اسید
- متانوییک اسید
- سولفوروس اسید
طبقه بندی اسیدها براساس منبع
اسیدها براساس منبع به دو گروه تقسیم می شوند : اسید معدنی – اسید آلی
این اسید از مواد معدنی تهیه می شوند و این اسیدها حاوی کربن نیستند مانند اسید سولفوریک – اسید کلریدریک، اسید نیتریک آشنایی با کاربرد اسید ها
کاربردها انواع اسید خود مبحث بسیار مفصلی است که ما در این صفحه بصورت مختصر برخی از کاربردهای اسید ها را در زندگی روزمره عنوان می کنیم:
- در صنعت نوشابه سازی در کشور ایران و تمامی کشورهای دنیا از اسید فسفریک استفاده به عنوان ماده اولیه استفاده می شود.
- در صنعت تولید انواع باطری ماشین از اسید سولفوریک رقیق شده با آب استفاده می شود.
- اغلب از اسیدها به منظور حذف زنگ زدگی و جلوگیری از خوردگی فلزات استفاده می کنند که در واقع به عنوان لعاب عمل می کنند.
- به عنوان الکترولیت در سلول مرطوب باتری مانند اسید سولفوریک در باتری خودرو مورد مصرف قرار می گیرند.
- در صنایع شیمیایی، برای واکنش های خنثی سازی به کار می روند.
- برای تولید نمک در واکنش های شیمیایی
- در صنایع غذایی به عنوان مکمل برای نوشیدنی ها و غذاها استفاده می شوند.
- به عنوان نگهدارنده در محصولات آرایشی و غذایی
- به عنوان کاتالیزورهای شیمیایی صنعتی و ارگانیک استفاده می شوند، برای مثال، اسید سولفوریک در تولیدات بنزین در مقادیر بسیار زیاد در فرایند آلکالایی استفاده می شود.
- در بیوشیمی نیز به عنوان کاتالیزور برای آنزیم ها از اسیدها استفاده می کنند.

کدام اسید قوی ترین است؟
برای شناخت قوی ترین اسید، باید در کنار توجه به شاخص PH موارد دیگری را هم در نظر گرفت. قوی ترین اسید، ماده ای است که اولا اسیدیته پایینی داشته باشد، ثانیا در مواجهه با آب، منجر به آزاد شدن هیدروژن بیش تری شود. قوی ترین اسید باید دریافت کننده الکترون باشد و هم چنین خاصیت خورندگی می تواند از دیگر شاخص هایی باشد که به قدرت اسیدها دامن می زند. تا مدت ها گمان می شد که سولفوریک اسید یا H2SO4 قوی ترین اسیدی است که شناخته شده است.
اما بعدها و با گسترش علم شیمی انواع اسید قوی تری شناخته شده اند که آنها را ابر اسید می نامند. اسید فلوئورانتیمونیک را می توان قوی ترین اسیدی معرفی کرد که شناخته شده است. این ماده با فرمول شیمیایی HSbF6 شناخته می شود و به قدری قوی است که می تواند شیشه را در خود حل کند.
این ماده از ترکیب دو اسید قوی هیدروژن فلوراید که فرمول شیمیایی آن HF می باشد و آنتیموان پنتافلوراید با فرمول شیمیایی SbF5 به دست می آید. به چنین ترکیباتی که از مخلوط شدن دو اسید قوی به دست می آیند، سوپر اسید گفته می شود. می توان اسید فلوئورانتیمونیک را به عنوان قوی ترین اسید شناخته شده معرفی نمود که به علت خاصیت خورندگی خود می تواند موارد استفاده فراوانی داشته باشد.
آشنایی با مفهوم اسید و باز
به طور کلی می توان همه مواد موجود در دنیا را در سه دسته اسیدی، قلیایی و خنثی جای داد. مواد اسیدی و بازی را می توان با شاخصی به نام PH یا اسیدیته سنجید. PH شاخصی است که بین 0 تا 14 متغیر می باشد. میانه این بازه یعنی عدد 7، به معنای خنثی بودن یک ماده است. اعداد بین 0 تا 7 بیان گر اسیدی بودن و شاخص بین 7 تا 14 بیان گر قلیایی بودن می باشد.
مواد اسیدی و بازی قوی و ضعیف را نیز می توان با همین شاخص سنجید. هر چه عدد شاخص اسیدیته به صفر نزدیک تر شود، ماده اسیدی تر است و هر چه به 14 نزدیک تر باشد، ماده مد نظر قلیایی تر می باشد. مواد اسیدی و بازی کاربردهای مخصوص به خود را دارند. در این بین اسیدها به علت خاصیت خورندگی بالا، کاربردهای عدیده ای هم در صنعت و هم در داروسازی و مواد غذایی پیدا کرده اند.
اسید خوراکی چیست؟
شاید برای شما جالب باشد که بدانید اسیدهایی وجود دارند که کاملا خوراکی هستند و در انواع صنایع تولید مواد غذایی به عنوان ماده اولیه مورد استفاده قرار می گیرند. از مهم ترین اسید اسیدها می توان به اسید سیتریک خوراکی اشاره کرد که در زبان عموم مردم به پودر جوهر نمک معروف می باشد.
از این اسید در صنعت تولید نوشابه، پاستیل، فرآورده های گوشتی، انواع آب میوه، لواشک و.... استفاده می شود.
اسید صنعتی چیست؟
اسید ها بیش ترین موارد استفاده خود را در بخش صنعتی دارند. غالبا از آنها به عنوان نوعی ماده پایه در تولیدات صنایع بهره گرفته می شود. در پاسخ به این پرسش که اسید صنعتی چیست باید گفت که هر نوع اسیدی که در صنعت مورد بهره برداری قرار می گیرد را اسید صنعتی می نامند.
می توان طیف گسترده ای از اسیدها را در این دسته بندی جای داد. به عنوان مثال هیدروکلریک اسید، اسید باتری، سولفوریک اسید، اسید استیک، اسید آنتیک کاری، فرمیک اسید، اگزالیک اسید، اسید نیتریک، اسید بوریک و ده ها اسید دیگر در این دسته بندی جای می گیرند. بخش های مختلفی از صنعت هستند که از این اسیدهای صنعتی برای تولید محصولات خود بهره می گیرند. معمولا اسیدهای صنعتی اسیدهای قوی هستند که می توانند به عنوان نوعی حلال و یا ماده اولیه تولید محصولات به کار آیند.
مرکز خرید اسید در اصفهان
شرکت داروسازی کیمیا اکسیر سازان کوثر به عنوان یکی از شرکت های بزرگ تولید و عرضه کننده انواع مواد شیمیایی و ضد عفونی کننده دامداری و مرغداری توانایی تامین نیاز مشتریان عزیز استان اصفهان به انواع اسید را بصورت عمده و خرد دارد. همچنین مجموعه ما قادر به تامین نیاز خریداران این محصول را در سراسر کشور دارد.
اسید خورنده چیست؟
اسید خورنده نیز به آن دسته یا گروهی از اسیدها گفته می شود که می توانند در صورت عدم احتیاط کاربران، مخاطره آمیز باشند و شرایط هولناکی را به وجود آورند. این عدم احتیاط و خطرات به وجود آمده ناشی از اسید کلریدریک، کلریدریک، هیدروفلوریک و.. است که می توانند به بدن، سلامتی و .. کاربران آسیب وارد کنند.
اثرات منفی و برآمده از ترکیبات خورنده و شیمیایی می توانند در اتباط با پوست و چشم باشد. بطوریکه هنگام تماس با این بخش های موضعی، موجب تحریک و سوزش فراوان می گردد. اثرات منفی دیگر آن ها مربوط به پوشش و بافت بینی، بافت گلو و دستگاه تنفسی می باشد. با استنشاق این ماده های خطرناک و خورنده، پیامد های نامطلوبی از جمله سوزش دستگاه تنفسی، گلو و… بروز پیدا می کند.
نحوه نام گذاری اسیدها چگونه است؟
در خصوص اکسواسیدها، پسوند (ییک+اسید) به نام اتم مرکزی افزوده میشود. مانند: فسفریک اسید یا نیتریک اسید. البته در برخی موارد اتم مرکزی مورد نظر بیش از یک نوع اکسواسید تولید میکند که تعداد اتم های اکسیژن هرکدام با دیگری متفاوت است. در این موارد، نام اسیدی که ظرفیت اتم مرکزی آن یک مرتبه از حالت معمول کمتر است با پسوند (و+اسید) مشخص میشود. مانند: سولفورو اسید و فسفرو اسید.
اگر تعداد اتم ها دو مرتبه از حالت معمول کمتر شود، پیشوند (هیپو) می گیرد. مثل: هیپوفسفرواسید. اگر تعداد اتم های اکسیژن اکسواسید، از حالت عادی یک عدد بیشتر باشد، پیشوند (پر) به آن افزوده خواهد شد. مانند: پرکلرواسید.
برای نامگذاری اسیدهای باینری یا دوتایی، پیشوند (هیدرو) را به نام نافلز آن می افزاییم و پسوند (ییک+اسید) را نیز به آن اضافه میکنیم. مثل: هیدروکلریک اسید.
نام اسیدهای آلی نیز در نتیجه ی افزودن پسوند (ییک+اسید) به نام آلکان تشکیل دهنده شان ساخته میشود. مانند: فرمیک اسید و سیتریک اسید.
در مورد تیواسیدها، پسوند (ییک+اسید) و پیشوند (تیو) به آنها اضافه می شود. بر اساس تعداد اتم های گوگرد موجود در ترکیب شیمیایی شان، پیشوند (دی) یا (مونو) میگیرند. مثل: مونوتیو فسفریک اسید و تیو سولفوریک اسید.

مدل فرمول نویسی اسیدها چگونه است؟
اسیدها همانند سایر ترکیبات از لحاظ بار الکتریکی خنثی می باشند یعنی بار الکتریکی آنیون و یون H برابر است.
اسیدهای تک پروتونی اسیدهایی هستند که هنگام حل شدن در آب فقط یک پروتون به مولکولH2O می دهند. از جمله اسیدهای تک پروتونه می توان اسید کلریدریک (HCl) رو نام برد. این نوع اسیدها فقط یک تفکیک برای آنها انجام می شود یعنی فقط یک ثابت تفکیک دارند.
اسیدهای چند پروتونی اسیدهایی هستند که در هنگام انحلال در آب چند پروتون به مولکول آب می دهند. از جمله این اسیدها می توان اسید فسفریک را نام برد که در زمان انحلال سه پروتون از دست می دهد. در اسیدهای چند پروتون دار از دست دادن پروتون طی یک مرحله تعادلی رخ می دهد و هر مرحله دارای ثابت تفکیک ویژه خود می باشد.
می شود گفت تمام اسیدهای چند پروتونی به استثنای اسید سولفوریک جزو اسیدهای ضعیف هستند. این نوع اسیدها بسته به تعداد H هایِ اسیدیشان یونش می یابند و طی هر مرحله یک هیدروژن از دست می دهند و همچنین در هر قسمت یونش مقدار Ka کوچک تر و PKa بزرگ تر از قسمت قبل است.
Ka(n)>Ka(n+1) و PKa(n)<PKa(n+1)
برای این نوع اسیدها در هر مرحله از دست دادن هیدروژن اسیدی سخت تر از مرحله قبل می شود. برای اینکه این موضوع را بهتر متوجه شوید مراحل یونش اسید فسفریک را برای شما شرح می دهیم.
H3PO4 + H2O ----> H2PO4 + H3O K = K1(H3PO4)
H2 PO4 + H2O ---->H PO42- + H3O K = K2(H3PO4)
HPO42- + H2O ----> PO43- +H3O K = K3(H3PO4)
همانطور که در این بخش، یونش اسید فسفریک را مشاهده می کنید به این نتیجه میرسیم که K1 بیشتر از K2 و K2 بیشتر از K3 است. نتیجه این فریند این است که جدا شدن پروتون از موکولی که بار ندارد آسان تر از جدا شدن یک پروتون از یک یون با یک بار منفی است. پس هرچه مقدار بار منفی بیشتر شود جدا شدن پروتون هم سخت تر می شود.
یک اسید چند پروتونی بسته به مقدار pH میتواند چند واکنش تفکیک داشته باشد. هر واکنش ثابت تفکیک ویژه خودش را دارد.
Ka1/ Ka2 /Ka3
H2 A(aq) + H2 O(l) ⇌ H3O+(aq) + HA−(aq) Ka1
HA−(aq) + H2 O(l) ⇌ H3O+(aq) + A۲−(aq) Ka2
ثابت تفکیک مرحله اول بیشتر از مرحله دوم است، یعنی Ka1> Ka2 برای مثال اسید سولفوریک میتواند یک پروتون بدهد و به آنیون بیسولفات تبدیل شود. هنگامی که Ka1 بسیاز بزرگ باشد، در این صورت میتواند دومین پروتون خود را بدهد و به آنیون سولفات تبدیل شود.
آنیون سولفات هم مقدار متوسطی دارد. مقدار بزرگ Ka1 در اولین تفکیک سبب می شود تا اسید سولفوریک، اسیدی قوی باشد. همانند این، مقدار کوچک کربنیک اسید میتواند اولین پروتون را بدهد و به آنیون بی کربنات تبدیل شود و دومین پروتون را بدهد و به کربنات تبدیل شود. هر دو مقدار Ka کوچک هستند اما داریم
Ka1> Ka2
یک مثال آلی از اسید سه پروتونی اسید سیتریک است، که میتوانند تمام پروتونهای خود را بدهد و در انتها به یون سیترات تبدیل شود.

موارد مصرف و کاربرد برخی از اسیدهای مهم
این اسید قوی می تواند به شکل رقیق شده در تولید اسید باتری به کار آید. هم چنین شاهد استفاده از آن در استخراج کانی های مورد نظر در معادن هستیم.اسید سولفوریک نوعی رسوب زداست که می تواند رسوبات ته نشین شده بر سطوح فلزی را به خوبی بزداید. هم چنین از این ماده در کشاورزی هم به کار می آید و می توان از آن به منظور تنظیم PH خاک به ویژه در باغات پسته بهره جست.
اصلی ترین کاربرد اسید نیتریک را می توان در زمینه استخراج طلا دانست. زیرا می تواند کلیه مواد به غیر از طلا را در خود حل کند و کار را برای استخراج طلا ساده سازد. هم چنین برای تولید مواد منفجره نظیر TNT هم از اسید نیتریک بهره گرفته می شود.
از دیگر اسیدها پر کاربرد هیدروکلریک اسید است. این اسید را می توان اسیدی دانسنت که به منظور تمیز کردن و گندزدایی در شوینده ها به کار برده می شود. به علت حضور یون کلر در این اسید می توان در گندزدایی استخرها و کلیه اماکنی که مستعد تجمع باکتری و قارچ ها هستند، از آن بهره جست.
یکی از اسیدهای ملایم می باشد که در تهیه مواد ضدعفونی کننده، حشره کش ها و حتی مواد دارویی و پمادهای سوختگی مورد استفاده قرار می گیرد.
این اسید قوی به عنوان ماده ای در تولید حشره کش ها، غنی سازی اورانیوم، تولید آلومینیوم، حکاکی روی شیشه و بسیاری از موارد دیگر کاربرد دارد.
اسید سولفامیک به عنوان یک ماده اصلی در تولید دارو، تمیز کننده های خانگی، تولید کاغذ، مایع لباس شویی و هم چنین تولید رنگ کاربرد دارد.
این اسید به عنوان افزودنی ارزان قیمت در نوشابه های گازدار مورد استفاده قرار می گیرد. هم چنین در گریدهای صنعتی مورد استفاده به عنوان کود شیمیایی می باشد.
کاربرد اسید کرومیک به علت خاصیت تمیز کنندگی ظروف آزمایشگاهی است. این ماده هم چنین در صنایع آبکاری مورد بهره برداری قرار می گیرد.
می توان اصلی ترین اسید در تولید رنگ، لاک، مواد پولیش خودرو، واکس و مواد آبکاری را اسید فرمیک دانست. هم چنین صنعت خوشبو کننده ها هم تا حد زیادی به این اسید وابسته است.

به منظور آبکاری فلزات و هم چنین ایجاد حالت آنتیک و عتیقه در آنها که این روزها به شدت طرفدار پیدا کرده است، از اسید آنتیک کاری بهره گرفته می شود.
این اسید به منظور تولید دارو و پمادهای ضد قارچ مورد بهره برداری قرار می گیرد. هم چنین صنعت تولید آفت کش ها و حشره ها کش ها از اسید بنزوئیک استفاده های فراوانی می کند.
از دسته اسیدهای خوراکی می توان به لاکتیک اسید اشاره کرد. این اسید در تولید محصولات لبنی، غذاهای کنسروی و ... به عنوان نوعی نگه دارنده استفاده می شود. هم چنین لاکتیک اسید استفاده های صنعتی هم دارد که اصلی ترین آن را می توان خاصیت رسوب زدایی آن دانست.
این اسید سفید کننده ای قوی است که از همین خاصیت آن بهره های فراوانی گرفته می شود. از استفاده در خمیر دندان ها به منظور سفید کنندگی تا صنعت به منظور سفید کردن تجهیزات صنایع می توان به کاربرد اگزالیک اسید اشاره کرد.
یکی از اسیدهای پر مصرف در صنعت باتری سازی، سولفونیک اسید است. این اسید به عنوان نوعی الکترولیت در صنعت باتری سازی مورد بهره برداری قرار می گیرد. هم چنین در صنعت رنگ و شوینده ها هم کاربرد دارد.